सामान्यतः प्रत्येक पदार्थ की तीन अवस्थाएं होती हैं; ठोस (Solid), द्रव (Liquid) एवं गैस (Gas)। साधारण ताप पर (At the Room Temperature i.e. 15-25°C) प्रत्येक पदार्थ इनमें से किसी एक अवस्था में पाया जाता है जिसे पदार्थ की सामान्य अवस्था (Normal State) कहते हैं। परन्तु गर्म करके ठोस को द्रव अवस्था में (जैसे-बर्फ को जल में) तथा द्रव को गैस अवस्था में (जैसे-जल को भाप में) बदल सकते हैं। इसके विपरीत ठण्डा करके गैस को द्रव अवस्था में (जैसे-भाप को जल में) तथा द्रव को ठोस अवस्था में (जैसे-जल को बर्फ में) बदल सकते हैं। इन प्रक्रियाओं को अवस्था परिवर्तन कहते हैं। ठोस से द्रव में परिवर्तन को गलन (Melting) तथा द्रव से गैस अथवा वाष्प (Vapour) में परिवर्तन को वाष्पन (Vaporisation) कहते हैं।
कुछ पदार्थ, जैसे- आयोडीन, नौसादर आदि गर्म करने पर ठोस अवस्था से सीधे गैस अवस्था में बदल जाते हैं। इस प्रक्रिया को ‘ऊर्ध्वपातन’ (Sublimation) कहते हैं।
अवस्था परिवर्तन पर दाब का प्रभाव (Effect of Pressure of the Change of State)
जो ठोस गलने पर आयतन में बढ़ते हैं जैसे- मोम, नेप्थलीन आदि, उनका गलनाँक (Melting Point) वाह्य दाब के बढ़ने पर कुछ बढ़ जाता है। इसके विपरीत जो ठोस गलने पर सिकुड़ते हैं जैसे- बर्फ, उनका गलनांक वाह्य दाब के बढ़ने पर कुछ कम हो जाता है।* किसी द्रव के क्वथनांक पर भी वाह्य दाब का प्रभाव पड़ता है। दाब कम होने पर क्वथनांक नीचा तथा दाब बढ़ने पर क्वथनांक ऊँचा (कुकर में) हो जाता है।*
• गलनांक (Melting Point)
ठोस का द्रव में परिवर्तन गलन (Melting) कहलाता है तथा जिस निश्चित ताप पर यह होता है उसे गलनांक कहते हैं। कोई अशुद्धि (Impurity) मिलाने पर गलनांक घट जाता है।*
• हिमांक (Freezing Point)
द्रव का ठोस में बदलना हिमीकरण (Freezing) तथा जिस निश्चित ताप पर द्रव ठोस में बदलता है उसे हिमांक कहते हैं। किसी पदार्थ का हिमांक व गलनांक प्रायः बराबर होता है।
• क्वथनांक (Boiling Point)
किसी द्रव के उबलने (Boiling) के कारण गैस या वाष्प में परिवर्तन को क्वथन तथा जिस निश्चित ताप पर यह होता है उसे क्वथनांक कहते हैं।
• वाष्पन (Vaporisation)
किसी द्रव के मुक्त सतह से कुछ अणु सदैव वाष्प या गैस में बदलते रहते हैं। इसे वाष्पन कहते हैं। यह प्रत्येक ताप पर होता है परन्तु ताप बढ़ने के साथ इसकी गति (Rate) बढ़ जाती है। क्वथन निश्चित ताप पर ही होता है।
द्रवणांक या संघनन बिंदु (Condensation Point) किसी गैस या वाष्प का द्रवीकरण, संघनन या द्रवण कहलाता है और जिस निश्चित ताप पर यह होता है उसे उस पदार्थ या गैस का द्रवणांक कहते हैं। किसी पदार्थ (matter) का द्रवणांक व क्वथनांक प्रायः समान होता है। जैसे-जल का द्रवणांक व क्वथनांक 100° सेल्सियस होता है।
➤ पुनर्हिमायन (Regelation)
यदि हम बर्फ के दो टुकड़ों को आपस में मिलाकर कुछ देर तक दबाएं, तो दबाव हटा लेने पर दोनों टुकड़े जुड़कर एक हो जाते हैं। इस घटना को पुनर्हिमायन (Regelation) कहते हैं। इसका कारण यह है कि जब टुकड़े मिलाकर दबाये जाते हैं तो मिलने के स्थान (Surface of Contact) पर दाब अधिक हो जाने के कारण, गलनांक (Melting Point) 0° सेल्सियस से कम हो जाता है। अतः उस स्थान पर बर्फ गलने (Melt) लगती है। दाब के हटा लेने पर गलनांक फिर बढ़ जाता है। अतः गली हुई बर्फ (ice) जमकर टुकड़ों को जोड़ देती है।
➤ गुप्त ऊष्मा (Latent Heat)
किसी पदार्थ का अवस्था परिवर्तन एक निश्चित ताप पर होता है तथा अवस्था परिवर्तन के समय ताप नियत (constant) रहता है। अतः नियत ताप पर सिर्फ अवस्था परिवर्तन हेतु आवश्यक ऊष्मा की मात्रा को पदार्थ की गुप्त ऊष्मा कहते हैं। अवस्था परिवर्तन दो प्रकार की होती है। यथा-
(a) गलन की गुप्त ऊष्मा (Latent Heat of Melting) नियत ताप पर किसी पदार्थ को ठोस से द्रव अवस्था में परिवर्तित करने हेतु आवश्यक ऊष्मा की मात्रा को उस पदार्थ के गलन की गुप्त ऊष्मा कहते हैं। जैसे- बर्फ से जल का बनना 0° सेल्सियस पर होता है और बर्फ के गलन की गुप्त ऊष्मा 80 किलो कैलोरी प्रति किग्रा होती है। अर्थात् 1 किग्रा बर्फ को जल में परिवर्तित करने हेतु 80 किलो कैलोरी ऊष्मा की आवश्यकता होती है। 1 किग्रा. जल को बर्फ बनाने के लिए भी 0° सेल्सियस पर जल से इतनी ही ऊष्मा (80 किलो कैलोरी) निकालनी पड़ती है।
(b) वाष्पन की गुप्त ऊष्मा (Latent Heat of Vaporisation)- नियत ताप पर किसी पदार्थ को द्रव से गैस (वाष्प) अवस्था में परिवर्तित करने हेतु आवश्यक ऊष्मा की मात्रा को उस पदार्थ के वाष्पन की गुप्त ऊष्मा कहते हैं। जल के वाष्पन (भाप) की गुप्त ऊष्मा 539 किलो कैलोरी/किग्रा होती है।
यदि किसी पदार्थ का द्रव्यमान m तथा गुप्त ऊष्मा L हो तो उस पदार्थ द्वारा एक निश्चित ताप पर अवस्था परिवर्तन में ली गई अथवा दी गई ऊष्मा,
Q = mL
➤ त्रिक बिन्दु (Triple Point)
किसी पदार्थ के ताप (T) तथा दाब (P) के बीच खींचे गये आरेख (Graph) को पदार्थ का प्रावस्था आरेख (Status Graph) या P-T आरेख कहते हैं।
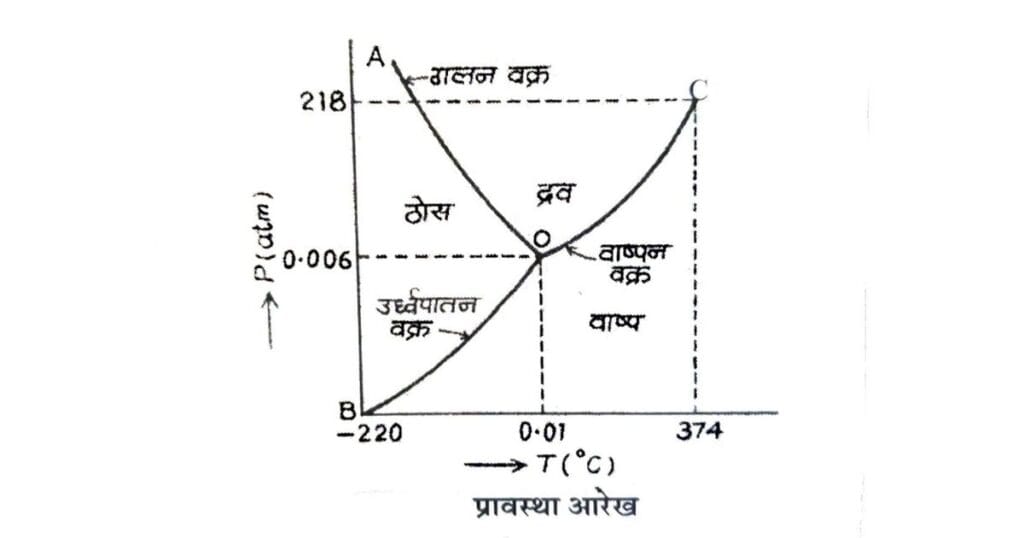
P-T आरेख, P-T तल को तीन क्षेत्रों ठोस, द्रव, गैस में विभाजित करता है। इन क्षेत्रों को तीन वक्रों गलन वक्र (OA), ऊर्ध्व पातन वक्र (OB) तथा वाष्पन वक्र (OC) द्वारा अलग किया जा सकता है। वह बिंदु (O), जहां तीनों वक्र मिलते हैं, पदार्थ का त्रिक बिंदु कहलाता है। अर्थात् त्रिक बिंदु पर पदार्थ की तीनों अवस्थाएं (ठोस, द्रव तथा वाष्प) साम्यावस्था (Equilibrium) में एक साथ रह सकती है। जल के त्रिक बिंदु पर ताप 0.01 °सेल्सियस तथा दाब 0.006 वायुमण्डल है जबकि कार्बन डाई आक्साइड (CO2) के त्रिक बिन्दु पर ताप 56.6°C तथा दाब 5.11 वायुमण्डल होता है।
क्रांतिक ताप (Critical Temperature)
किसी पदार्थ का क्रांतिक ताप वह ताप होता है जिसके ऊपर ताप होने पर पदार्थ को केवल दाब डालकर कभी भी द्रवित (liquidise) नहीं किया जा सकता। उपर्युक्त चित्र में वाष्पन वक्र पर प्रदर्शित बिंदु C पर ताप, क्रांतिक ताप को प्रदर्शित करता है। जल के लिए इसका मान 374°C तथा CO2 के लिए 31.1°C होता है।
➤ हिम मिश्रण (Freezing Mixture)
सामान्यतः किसी पदार्थ में कोई अशुद्धि (Impurity) मिलाने पर उसका गलनांक (Melting Point) कम हो जाता है। जैसे- यदि 0°C पर पिघलती बर्फ में कुछ नमक, शोरा आदि मिलाने पर बर्फ का गलनांक घटकर -22°C तक पहुँच जाता है। इसका कारण यह है कि जब बर्फ (ice) में नमक मिलाया जाता है तब नमक को 0°C तक ठंडा करने में कुछ बर्फ गल जाती है। इससे प्राप्त जल में नमक का विलयन (Solution) बन जाता है जिसका हिमांक शुद्ध जल के हिमांक से कम होता है। अतः बर्फ 0°C पर नमक के घोल के संपर्क में गलने लगती है तथा इसके लिए आवश्यक गुप्त ऊष्मा मिश्रण से ले लेती है जिससे विलयन का ताप गिर जाता है। इस पिघली बर्फ में और नमक घुलता है और उक्त क्रिया फिर दुहराई जाती है इस तरह जब मिश्रण का ताप -22°C तक पहुँच जाता है तो बर्फ नमक के घोल के साथ ठोस अवस्था में रह सकती है। अतः मिश्रण का ताप और नहीं गिरता। इसे ही हिम मिश्रण कहते हैं। गर्मियों में इसी विधि से आइसक्रीम, कुल्फी आदि जमाई जाती है।
➤ आर्द्रता (Humidity)
वायुमण्डल में उपस्थित जलवाष्प की मात्रा को आर्द्रता (Humidity) कहते हैं तथा वायुमण्डल में उपस्थित जलवाष्प की मात्रा तथा दाब के प्रभावों का अध्ययन आर्द्रतामिति कहलाता है।
➤ आपेक्षिक आर्द्रता (Relative Humidity)
किसी निश्चित ताप पर वायु के किसी आयतन (Volume) में उपस्थित जल वाष्प की मात्रा तथा उसी ताप पर उसी आयतन की वायु को संतृप्त (Saturated) करने के लिए आए जलवाष्प की मात्रा के अनुपात को आपेक्षिक आर्द्रता कहते हैं। प्रतिशत में व्यक्त करने के लिए इसमें 100 से गुणा कर देते हैं। अर्थात् आपेक्षिक आर्द्रता =
(किसी ताप पर वायु के किसी आयतन में जलवाष्प की मात्रा)/(उसी ताप पर उसी आयतन की वायु को संतृप्त करने के लिए आवश्यक जल वाष्प की मात्रा)×100
आपेक्षिक आर्द्रता का मान ताप बढ़ने पर बढ़ जाता है। आपेक्षिक आर्द्रता अधिक होने पर वर्षा होने की संभावना होती है। इसकी माप करके मौसम विज्ञानी मौसम पूर्वानुमान (weather forcasting) प्रस्तुत करते हैं।*
➤ कोहरा या कुहासा (Fog or Mist)
जाड़ों में जब वायुमण्डल का ताप गिर जाता है तो ऊपर की वायु ठण्डी होकर संतृप्त हो जाती है तथा यह जलवाष्प धूल (dust particles) व धुएँ के कणों (Smoke particles) पर संघनित (Condense) होकर छोटी-छोटी बूँदों में परिवर्तित हो जाती है जिससे वायुमण्डल में दूर तक देखना मुश्किल हो जाता है। इसे ही कोहरा (Fog) कहते हैं।
➤ ओस (Dew)
दिन के अधिक ताप में वायु अधिक आर्द्रता ग्रहण करने में सक्षम होती है परन्तु रात्रि में जब वायु का ताप कम हो जाता है तो वायु जलवाष्प की उसी मात्रा से संतृप्त (Saturated) हो जाती है।
थोड़ा और ताप कम होने पर वायु की आर्द्रता ग्राही क्षमता (Moisture Absorbing Capacity) और कम हो जाती है जिससे अतिरिक्त जलवाष्प (Moisture) संघनित होकर छोटी-छोटी बूँदों के रूप में पत्तियों पर जमा हो जाती हैं जिन्हें ओस कहते हैं।
➤ पाला (Frost)
जाड़े की रात्रि में जब बहुत अधिक ठण्ड होने पर पृथ्वी के आस-पास की वायु का ताप 0°C तक गिर जाता है तो जल वाष्प पेड़ों की पत्तियों पर संघनित होने के साथ-साथ जम (Freeze) भी जाती है जिन्हें हम बर्फ के छोटे टुकड़ों के रूप में देख सकते हैं। इसे ही पाला (Frost) कहते हैं। कभी-कभी इससे पौधों की नसों (Veins) व कोशिकाओं (Cells) में उपस्थित जल भी जम जाता है जिससे कोशिकाएं व तना फट जाता है और पौधा सूख जाता है।
➤ बादल तथा वर्षा (Clouds and Rain)
गर्मियों में जल नदियों, तालाबों तथा समुद्र आदि से वाष्पीकरण (Vaporisation) द्वारा वाष्प बनकर उड़ जाता है। वायुमण्डल में लगभग 100 मीटर की ऊँचाई पर हवा का ताप लगभग 1°C कम हो जाता है। ज्यों-ज्यों ऊपर जाते हैं, वायुदाब तथा वायु का ताप दोनों कम होते जाते हैं। जल वाष्प (Moisture) भरी हवाएँ जब ऊँचाई पर पहुँचती हैं तो उनका भी ताप कम होने लगता है। एक ऐसी स्थिति आती है कि जलवाष्प बहुत ही छोटी-छोटी जल की बूँदों के रूप में हवा में उड़ते धूल के कणों (dust particles) के ऊपर जम जाती है। इन्हें हम बादल बनना कहते हैं।
यदि हवा में पर्याप्त बादल बन जाते हैं और हवा का ताप घटता जाता है तो छोटी – छोटी बादल की बूँदें बड़े आकार की हो जाती हैं, जिसका भार धूल के कण नहीं संभाल पाते। ये बूंदें पृथ्वी पर आने लगती हैं, जिन्हें हम वर्षा (Rain) कहते हैं।
यह भी पढ़ें : ऊष्मा स्थानान्तरण (Heat Transmission)

1 thought on “अवस्था परिवर्तन तथा गुप्त ऊष्मा (Change of State and Latent Heat)”